國人對於骨骼健康的關注主要來自骨質疏鬆症,此疾病是一種與老化相關的全身性骨病變,患者因骨穩態失衡和骨微觀結構破壞導致骨密度和骨質下降,導致較常人更容易發生骨折。飲食中的營養素與骨質疏鬆症的發生率相關,維生素D、鈣與鎂,是骨骼健康的關鍵調節劑,並對骨質疏鬆症風險有明顯影響。
骨骼透過破骨細胞和成骨細胞之間的協調和相互作用不斷重塑,以達到骨穩態,在此過程中,鈣與鎂扮演重要角色。本文的重點,將探討鈣與鎂調控造骨的機制,以及可應用於保護骨骼健康的型態。
鈣訊號傳遞與鈣離子通道調控造骨作用
原發性骨質疏鬆症包括停經後和老年性骨質疏鬆症,主要歸因於雌激素水平下降和老化過程。骨質疏鬆症的主要病理機轉,則是破骨細胞過度活化,增加骨吸收。鈣訊號傳遞可以調節破骨細胞活化,其訊號傳遞若中斷,破骨細胞介導的骨吸收將增加,進而促進骨質疏鬆症的進展。
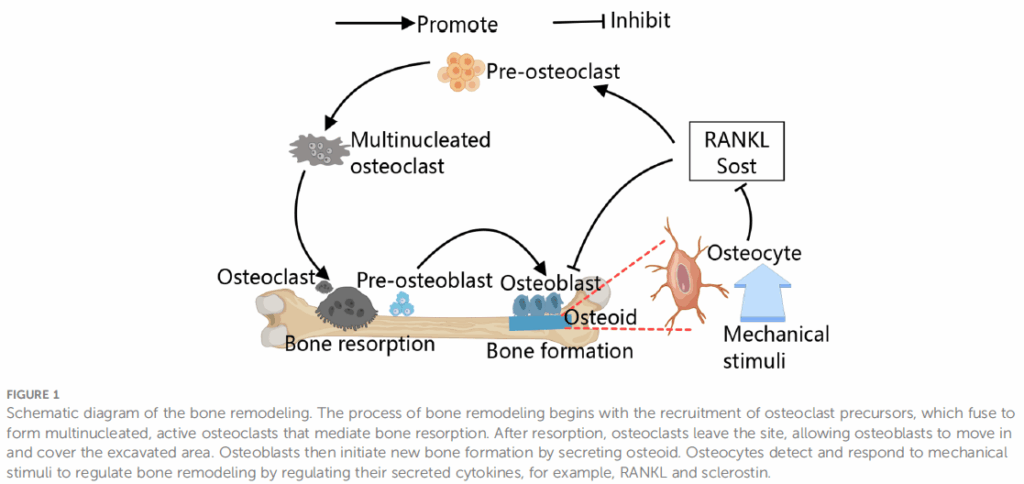
下圖來自2024年的期刊1,描述骨重塑過程。首先由破骨細胞前驅細胞的聚集,融合形成多核、活化的破骨細胞,來執行骨吸收。骨吸收完成後,破骨細胞離開原位,改由成骨細胞進入該區域,透過分泌類骨質來形成新骨。
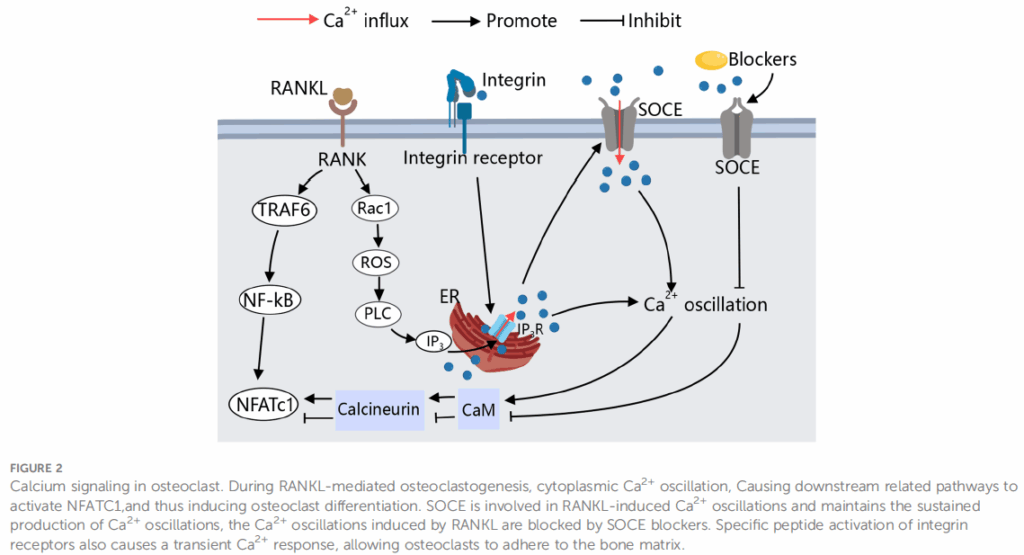
來自同論文的另一張圖,描述破骨細胞中的鈣訊號傳遞。RANKL/RANK訊號路徑會活化磷脂酶C (PLC),產生肌醇1,4,5-三磷酸(IP3),與內質網(ER)上的肌醇1,4,5-三磷酸受體(IP3R)結合,引發鈣離子振盪。這導致鈣離子與鈣調蛋白(CaM)結合,活化鈣調神經磷酸酶,後者使NFATc1去磷酸化,進而促進破骨細胞分化。SOCE訊號路徑,可共同調控RANKL誘導的鈣離子振盪,並維持鈣離子振盪的持續產生。當使用SOCE阻斷劑時,RANKL與SOCE路徑的鈣離子振盪都會終止。
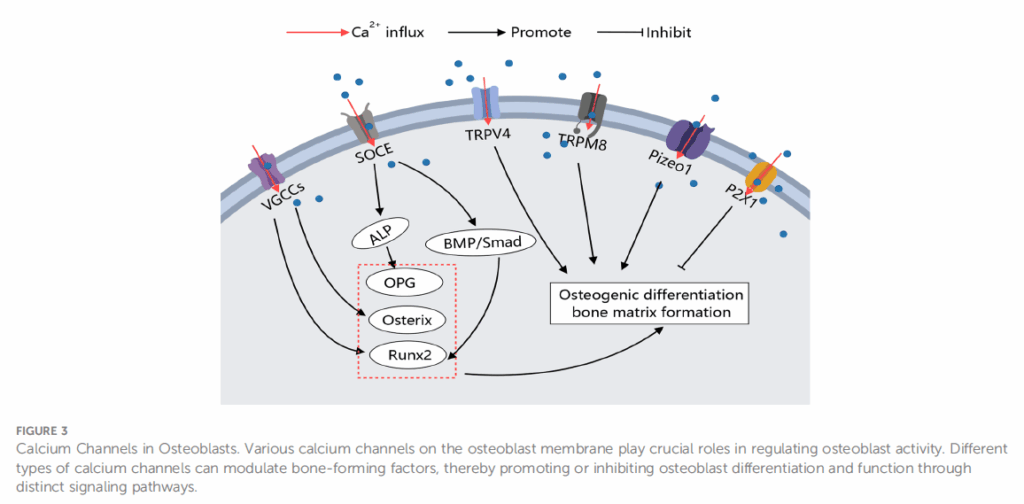
來自同論文的另一張圖,描述成骨細胞中的鈣通道。成骨細胞膜上的各種鈣通道在調節成骨細胞活性中發揮著至關重要的作用。不同類型的鈣通道可以調節骨形成因子,從而透過不同的訊號路徑促進或抑制成骨細胞的分化和功能。例如,VGCCs廣泛存在於成骨細胞中,並被細胞外環境的變化(例如高濃度的鈣)激活,從而促進成骨分化;TRPM8已被證實能夠促進骨髓間質幹細胞的成骨分化;一些研究則發現,SOCE和Piezo通道的活化,可以減輕骨質疏鬆症的症狀。
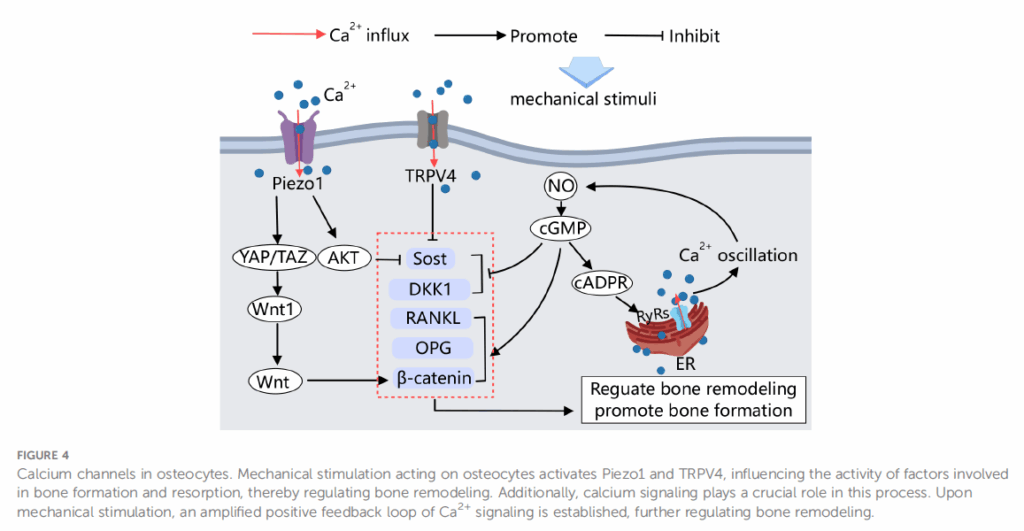
來自同論文的另一張圖,描述骨細胞中的鈣通道。骨細胞是機械負荷敏感細胞,參與骨形成、適應和骨吸收,以回應機械負荷。在骨微環境中,骨細胞被包裹在細胞膜和堅硬骨基質界面處的細胞周圍基質中,各種機械刺激,包括壓縮、拉伸和扭轉,因為空間變形而從細胞外液流動產生流體剪切力,可以活化細胞周圍基質中的骨細胞之離子通道,例如Piezo1和TRPV4,啟動了一系列下游路徑來調節骨重塑。此外,機械刺激會建立鈣訊號正向回饋,進一步增強骨形成。
鎂調控造骨並改善骨質疏鬆
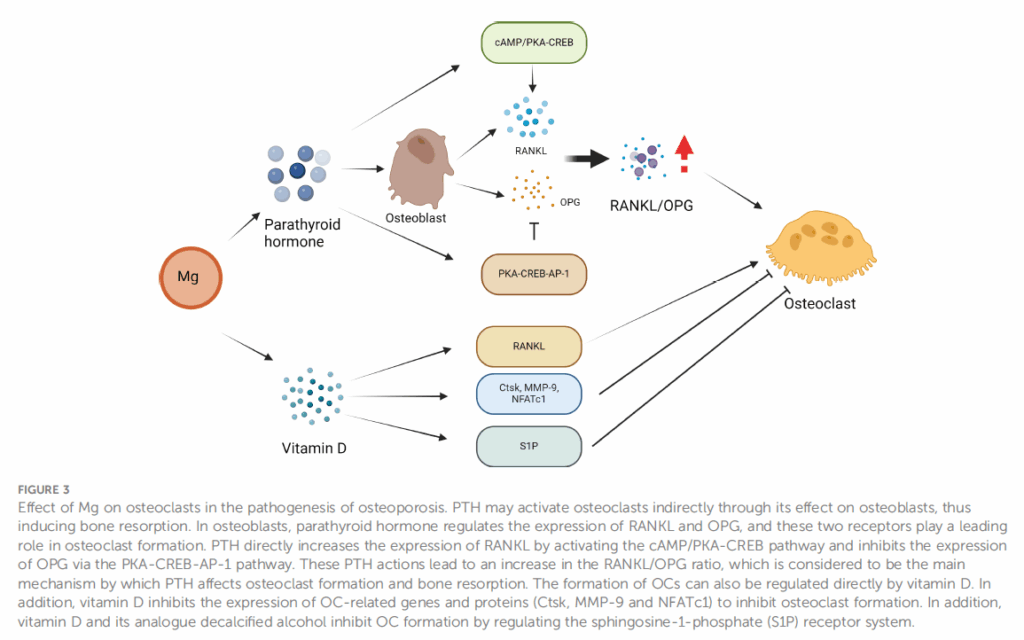
鎂與鈣同是骨骼發育和礦化所必需的營養元素,在骨質疏鬆症的進展中起著重要作用。下圖來自2024年的期刊2,描述鎂對破骨細胞的影響。高濃度的鎂會抑制副甲狀腺素(PTH)的分泌,由PTH抑制破骨細胞活性與骨吸收。反之,鎂缺乏的狀態下,副甲狀腺素透過活化cAMP/PKA-CREB路徑直接增加RANKL的表達,並透過PKA-CREB-AP-1路徑抑制OPG的表達。當成骨細胞RANKL/OPG比值升高時,將間接活化破骨細胞與骨吸收,從而加速骨質疏鬆症的進展。此外,鎂缺乏症患者通常血清維生素D濃度較低,維生素D可透過抑制骨鈣化相關基因(Ctsk、MMP-9和NFATc1)的表達,或透過調節S1P受體系統,來抑制破骨細胞的形成。
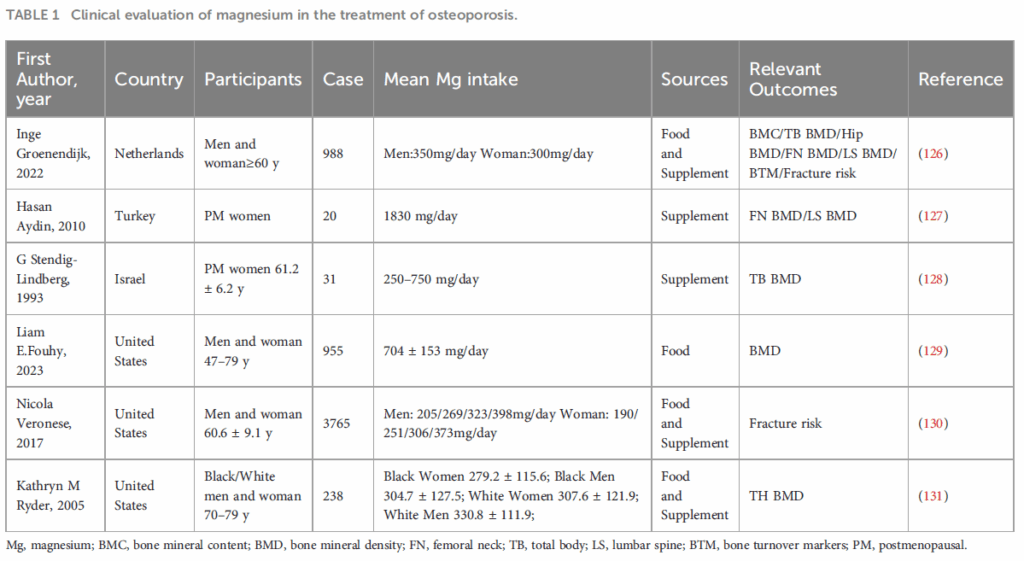
來自同論文的另一張表,列出補充鎂改善骨質疏鬆症影響之臨床研究,測試對象包含停經後女性或老年人,其統合分析結果相當一致。鎂攝取量與骨密度(BMD)之間存在顯著的正相關性,部位包含:髖關節、股骨、頸骨等,但與腰椎骨密度之間較無顯著相關性。
鎂於骨科醫療材料的應用
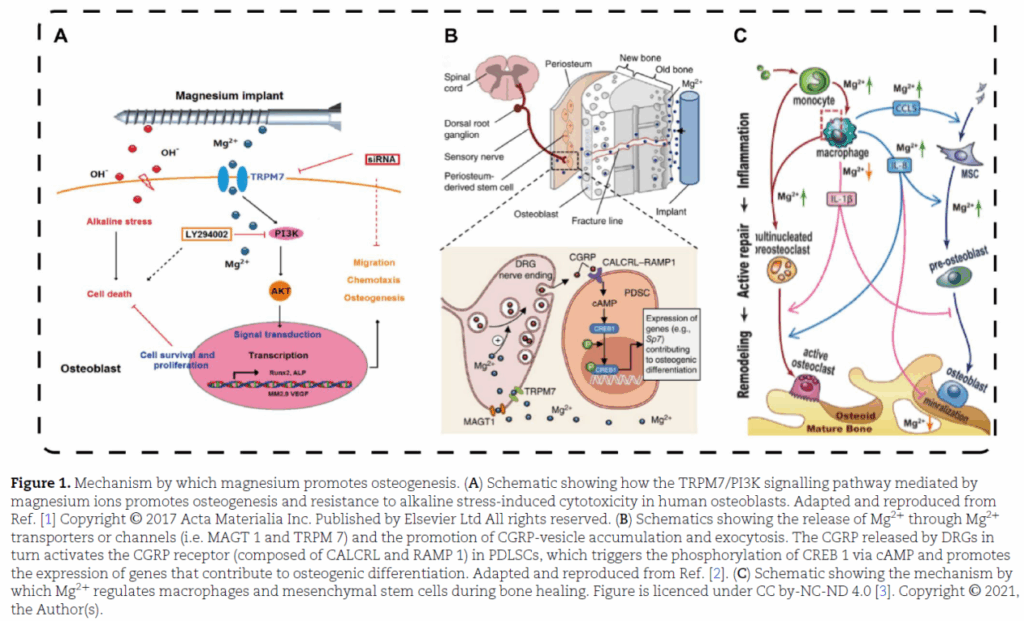
可生物降解的鎂基材料作為骨科植入物,因其良好機械性質、生物相容性與分解速率而佔盡優勢,臨床研究均一致表明,鎂還具有促進骨組織形成的能力。下圖來自2025年的期刊3,推論鎂材料降解時釋放的鎂離子,對於環境中的多種細胞可能產生之作用: A、鎂離子透過TRPM7/PI3K訊號路徑,活化成骨細胞,並減少鹼性環境造成的細胞損傷。B、鎂離子透過神經細胞的鎂離子轉運體通道(即MAGT 1和TRPM 7),誘發CGRP囊泡進行胞吐,從而透過牙周膜細胞的cAMP觸發CREB 1的磷酸化,促進成骨相關基因的表達。C、鎂離子透過間質幹細胞和巨噬細胞,間接調節破骨細胞與成骨細胞進行之骨癒合。
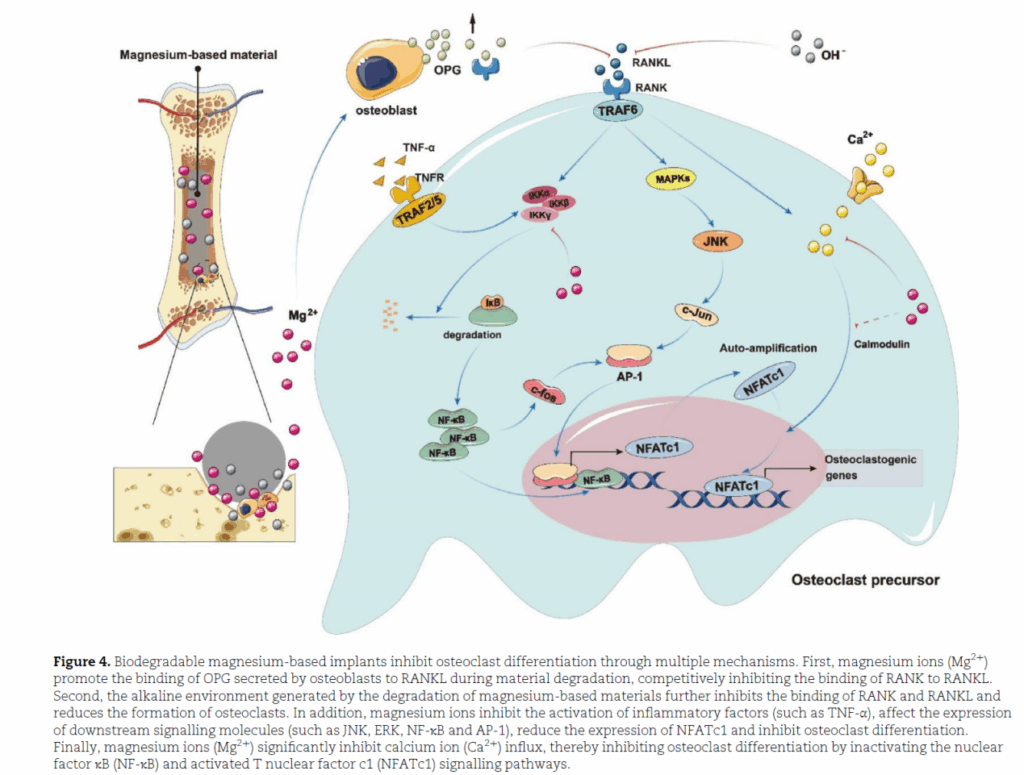
來自同論文的另一張圖,描述可生物降解鎂基植入物透過多種機制抑制破骨細胞活化。OPG/RANK/RANKL訊號路徑對於調控破骨細胞至關重要,鎂離子在材料降解過程中促進成骨細胞分泌的OPG與RANKL結合,競爭性抑制RANKL與RANK結合,故而減少破骨細胞活化。其次,鎂降解產生的鹼性環境亦可抑制RANKL與RANK的結合,貢獻相似效益。此外,鎂離子抑制發炎因子(如TNF-α)的活化,影響下游訊號分子如JNK 、AP-1和NF-κB,降低NFATc1的表達,故而抑制了破骨細胞分化。
總結
在骨骼的重塑過程中,破骨細胞的骨吸收和成骨細胞的骨形成相互耦合,如果骨吸收超過骨形成,就會發生骨質疏鬆症等骨骼疾病。在骨重塑過程的局部微環境,其特徵是細胞外鈣濃度的劇烈波動,由破骨細胞先進行骨吸收,使附近的組織液鈣濃度會從生理體液中的1.8 mM升高到5 mM,局部鈣離子濃度最高可達40 mM,遠高於正常血漿總鈣濃度(2.25-2.5 mM)。升高的鈣濃度有利於成骨細胞活化,使其在局部微環境中持續生成骨。在破骨細胞與成骨細胞上有各種鈣離子通道,可以感知並產生鈣訊號傳遞,決定破骨細胞與成骨細胞的後續反應。破骨細胞有RANK、SOCE等鈣離子通道,成骨細胞則有VGCCs、TRPM8等鈣離子通道,這些鈣通道可能作為治療骨質疏鬆症的潛在治療策略。
鎂對於造骨的調控,不像鈣可以直接透過鈣離子通道來作用,而是透過副甲狀腺素和維生素D來影響RANK/RANKL/OPG訊息路徑,間接影響骨骼結構。多項臨床研究表明,補充鎂可以在一定程度上緩解骨質疏鬆症的症狀。除了膳食補充劑的型態,鎂還可以作為生物可分解的骨科植入物,降解過程產生的高濃度鎂離子,已被證明能夠增強成骨細胞活性,同時抑制破骨細胞的形成,對骨重塑發揮關鍵治療作用。
參考文獻
The role of calcium channels in osteoporosis and their therapeutic potential. Ying Hao, Ningning Yang, Mengying Sun, Shangze Yang and Xingjuan Chen. PUBLISHED 07 August 2024. DOI 10.3389/fendo.2024.1450328.
The role of magnesium in the pathogenesis of osteoporosis. Lin Liu, Pan Luo, Pengfei Wen and Peng Xu. Frontiers in Endocrinology. PUBLISHED 06 June 2024. DOI 10.3389/fendo.2024.1406248.
Research progress on osteoclast regulation by biodegradable magnesium and its mechanism. Wangwei Zhu, Weidan Wang, Xing Yang, Chunxiao Ran, Tianwei Zhang, Shibo Huang, Jiahui Yang, Fuyang Wang, Huiya Wang, Peng Wan, Fengyuan Piao, Faqiang Lu, Shengbo Shi, Ye Li, Xiuzhi Zhang and Dewei Zhao. Regenerative Biomaterials, 2025, 12, rbaf026.

