退化性關節炎(osteoarthritis, OA)是一種高度盛行、與老化及慢性發炎相關的退行性關節疾病,其病理特徵包括軟骨基質分解、滑膜發炎、軟骨下骨重塑異常,以及氧化壓力失衡。近年研究顯示,微量元素鋅(zinc)在 OA 的發生與進展中扮演關鍵但複雜的角色。鋅不僅是多種抗氧化與免疫調控蛋白的重要輔因子,也可透過鋅轉運蛋白與轉錄因子參與軟骨代謝與發炎訊號調控。然而,過量或鋅訊號失衡亦可能促進基質降解與關節退化。本文將系統性探討鋅在 OA 中的雙重角色,聚焦其分子與細胞層級的調控機制,並評估其於臨床應用上的潛力與限制,進而提出「精準調控鋅生物可用度」作為未來 OA 營養與輔助治療策略的重要方向。
退化性關節炎與微量元素調控的興起
退化性關節炎是最常見的慢性關節疾病之一,隨著人口老化,其盛行率與醫療負擔持續攀升。OA 長期被視為單純的「磨損性疾病」,然而近十餘年的研究已明確指出,慢性低度發炎、氧化壓力、細胞代謝失衡與免疫調控異常,共同驅動 OA 的病理進程。
在此背景下,營養因子與微量元素對關節健康的影響逐漸受到重視。鋅作為人體必需微量元素,參與超過 300 種酵素與數千種轉錄因子的結構與功能調控,其在免疫調節、抗氧化防禦與組織修復中的角色,使其成為 OA 研究的重要焦點。
鋅的生物學功能與關節微環境中的角色
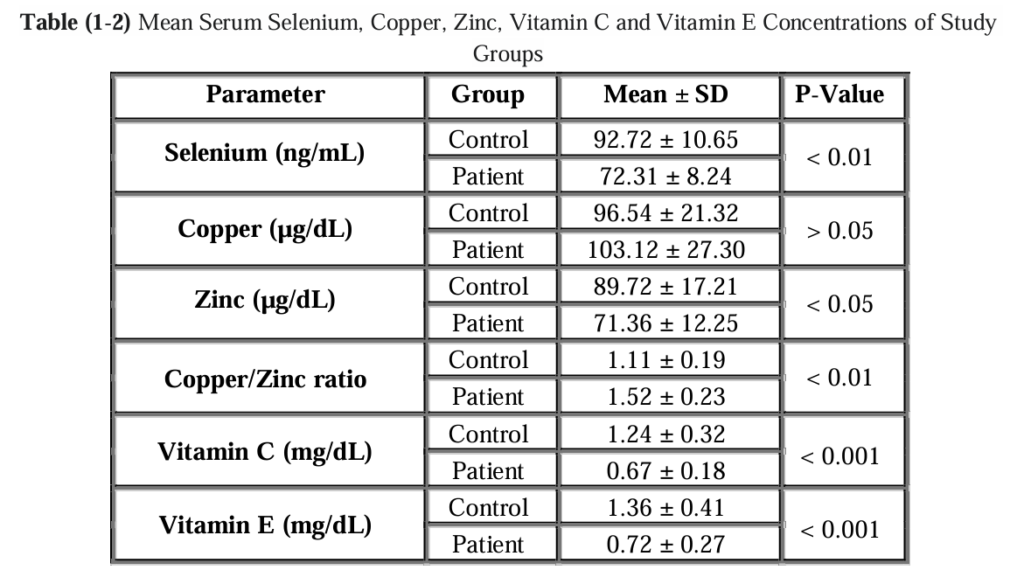
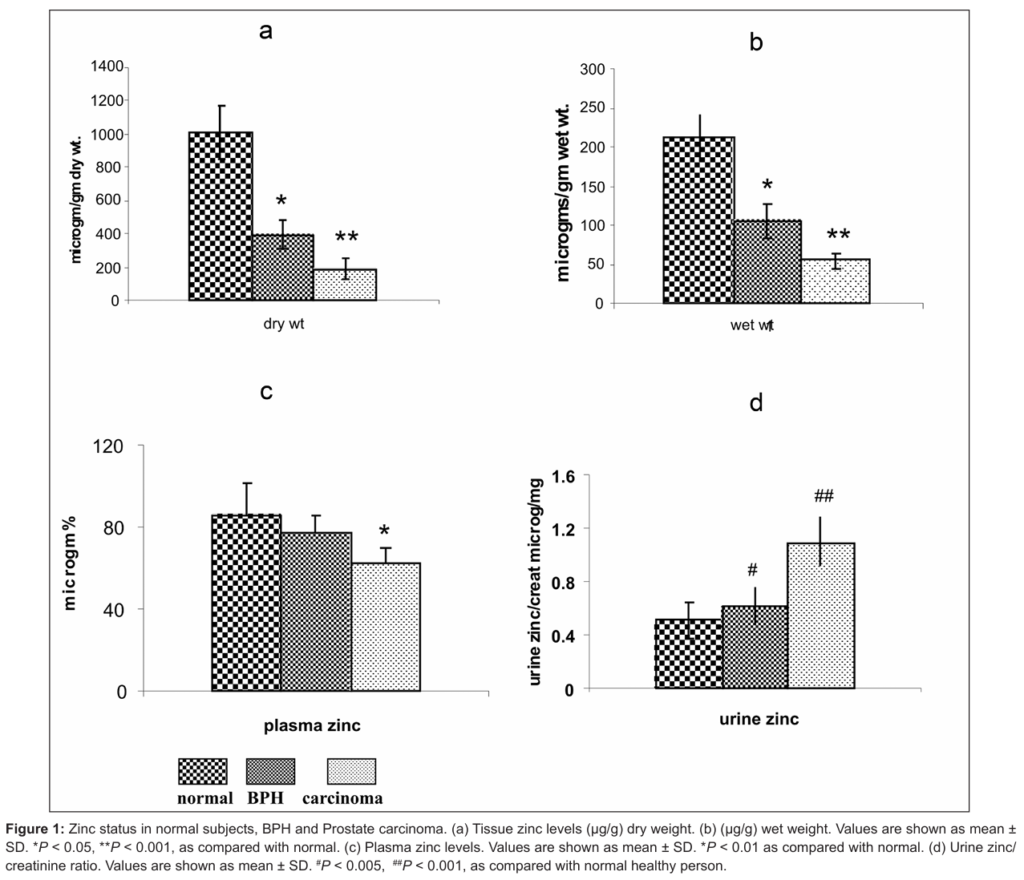
近年研究亦指出,退化性關節炎並非單一營養因子失衡所致,而是關節局部微環境中多種微量元素共同參與的結果。Amhare 等人於 2025 年發表之綜述,系統性整理鋅、銅與硒在 OA 病理中的角色,指出這些元素透過調控氧化壓力、慢性發炎反應與軟骨細胞存活,共同影響關節結構的穩定性。其中,鋅被認為是連結抗氧化防禦與免疫調節的重要節點,其動態平衡對於維持軟骨代謝與延緩退化具有關鍵意義。該整合模型顯示,微量元素失衡可能放大發炎與基質降解訊號,進而加速 OA 的進展。(Figure 1. Amhare et al., Nutrients, 2025)
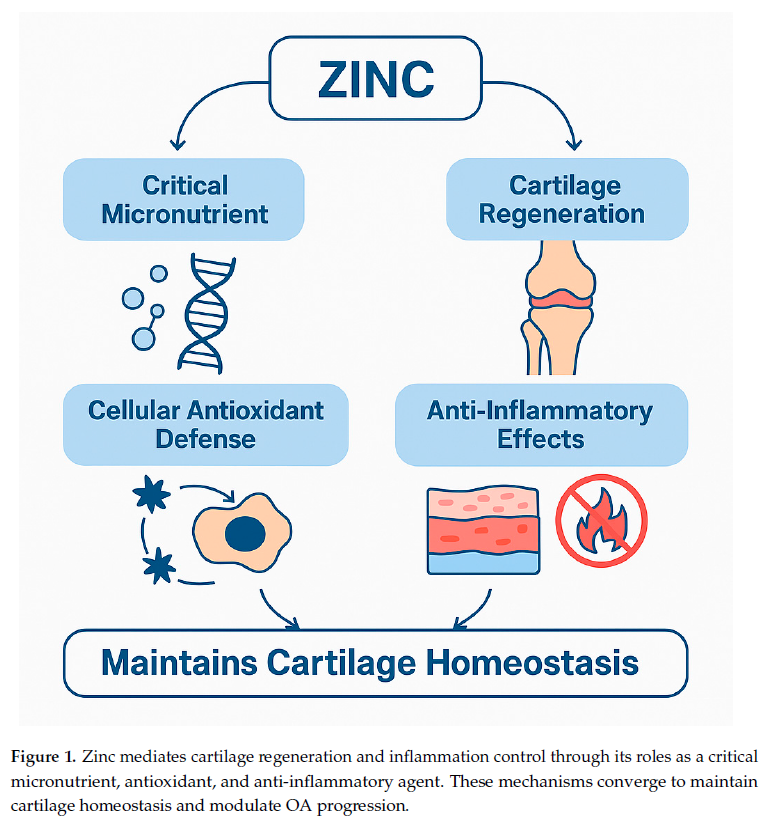
鋅在體內並非僅作為結構性元素,而是透過「可交換鋅池(labile zinc pool)」參與細胞訊號調控。於關節組織中,鋅影響下列關鍵過程:
-
抗氧化防禦系統
鋅是超氧化物歧化酶(Cu/Zn-SOD)等抗氧化酵素的重要組成,能間接降低活性氧(ROS)累積,而 ROS 被認為是促進軟骨細胞老化與基質分解的重要因子。
-
免疫與發炎調控
鋅可調節 NF-κB、MAPK 等發炎訊號路徑,影響 IL-1β、TNF-α 等關節發炎細胞激素的表現,進而影響 OA 的炎症微環境。
-
軟骨基質穩定性
軟骨細胞(chondrocytes)中的鋅動態,與基質合成與分解酵素的平衡密切相關。
上述鋅訊號在生理條件下有助於關節穩態維持,但在病理狀態下,亦可能被重新導向至促進基質分解的訊號路徑。
鋅於退化性關節炎中的分子與細胞調控機制
鋅的抗氧化與抗發炎作用
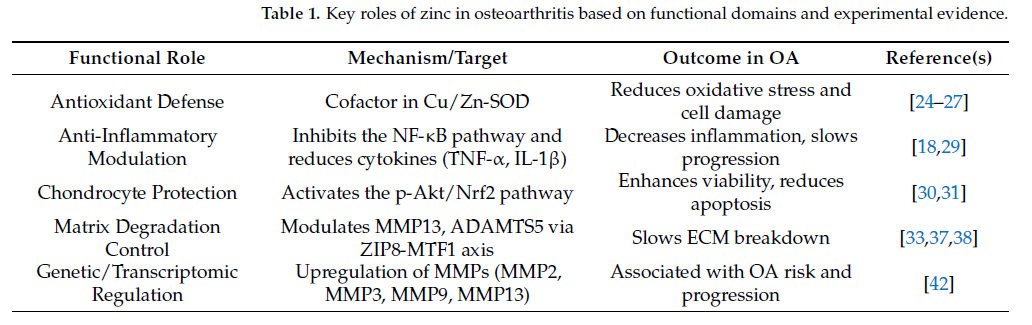
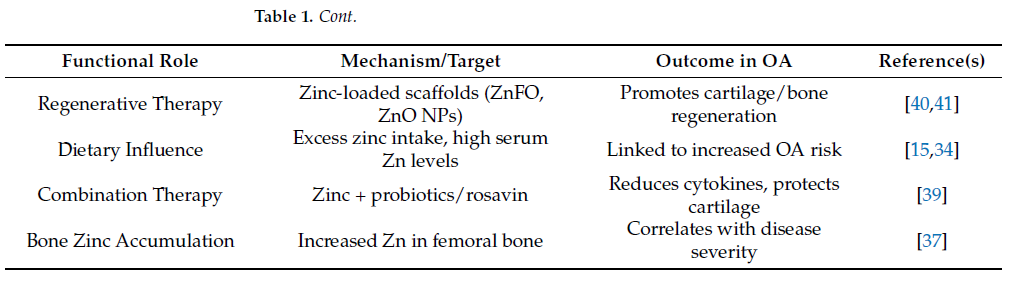
多項細胞與動物研究顯示,在 OA 條件下,鋅可透過活化 Akt/Nrf2 抗氧化訊號軸,提升細胞對氧化壓力的耐受性。Nrf2 活化後,誘導下游抗氧化酵素表現,減少 ROS 所誘發的軟骨細胞凋亡與基質破壞。此外,鋅亦可抑制促發炎轉錄因子 NF-κB 的活化,降低發炎介質對軟骨的長期傷害,顯示其在 OA 早期與中期可能具有保護作用。(Table 1. Amhare et al., Nutrients, 2025)
鋅轉運蛋白與基質分解的雙面刃效應
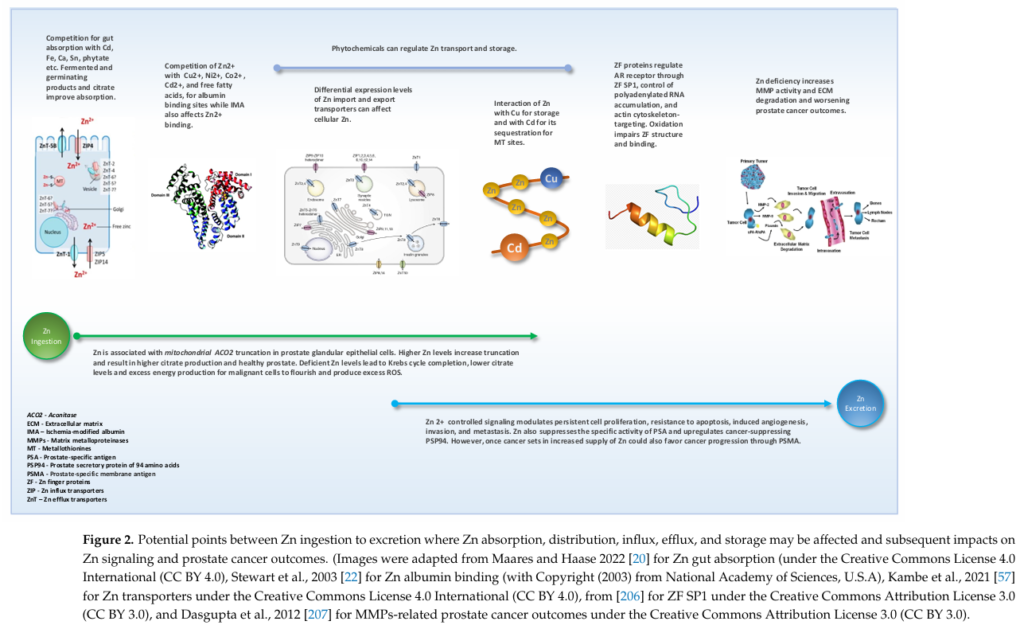
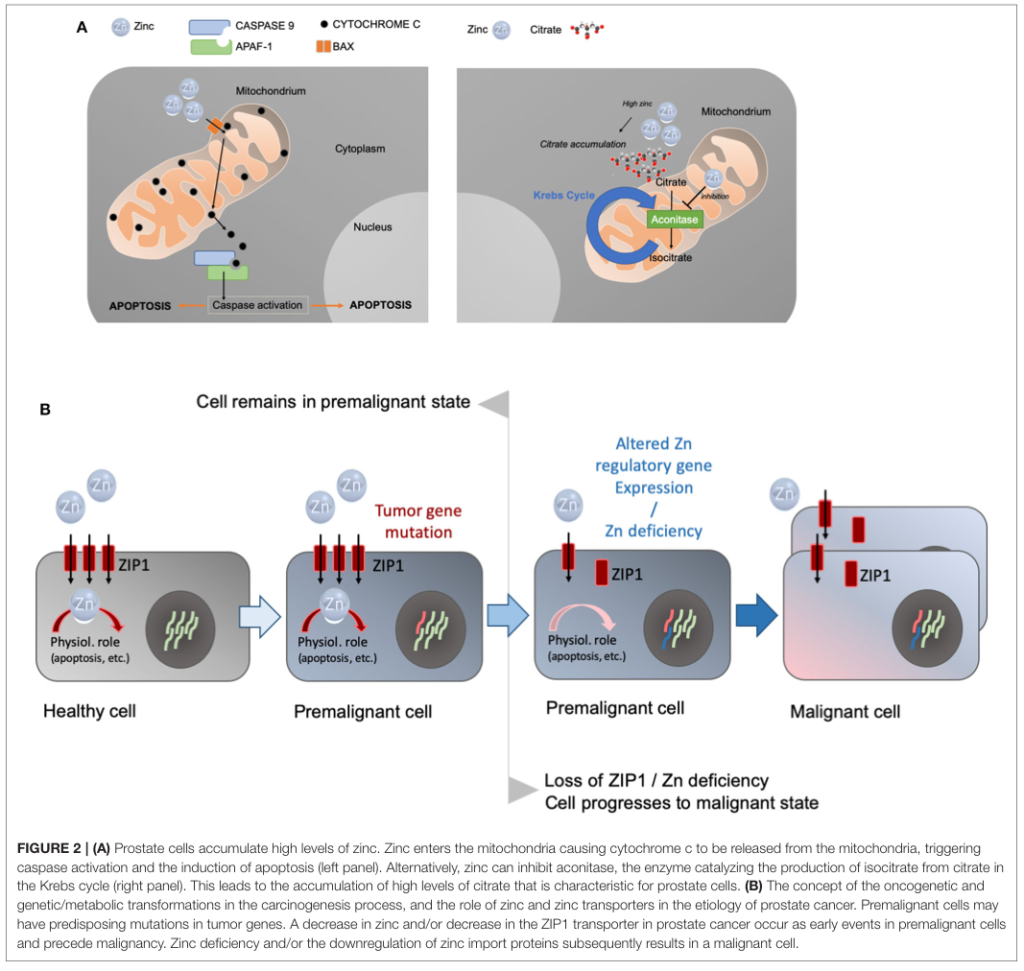
在分子層級上,鋅於退化性關節炎中的作用並非僅止於抗氧化或免疫調節。Kim 等人於 Cell 發表的研究指出,在 OA 病理條件下,軟骨細胞中鋅轉運蛋白 ZIP8 顯著上調,導致細胞內游離鋅濃度增加。此一鋅訊號並非被動累積,而是作為轉錄調控訊號,活化金屬反應轉錄因子 MTF1,進而誘導多種基質分解相關基因(如 MMP3、MMP13)之表現,形成促進軟骨基質降解的分子級聯反應。此研究揭示,鋅在 OA 中可透過特定轉運與轉錄軸線,轉化為病理性訊號放大因子,凸顯鋅動態調控的重要性。(Figure 4. Kim et al., Cell, 2014)
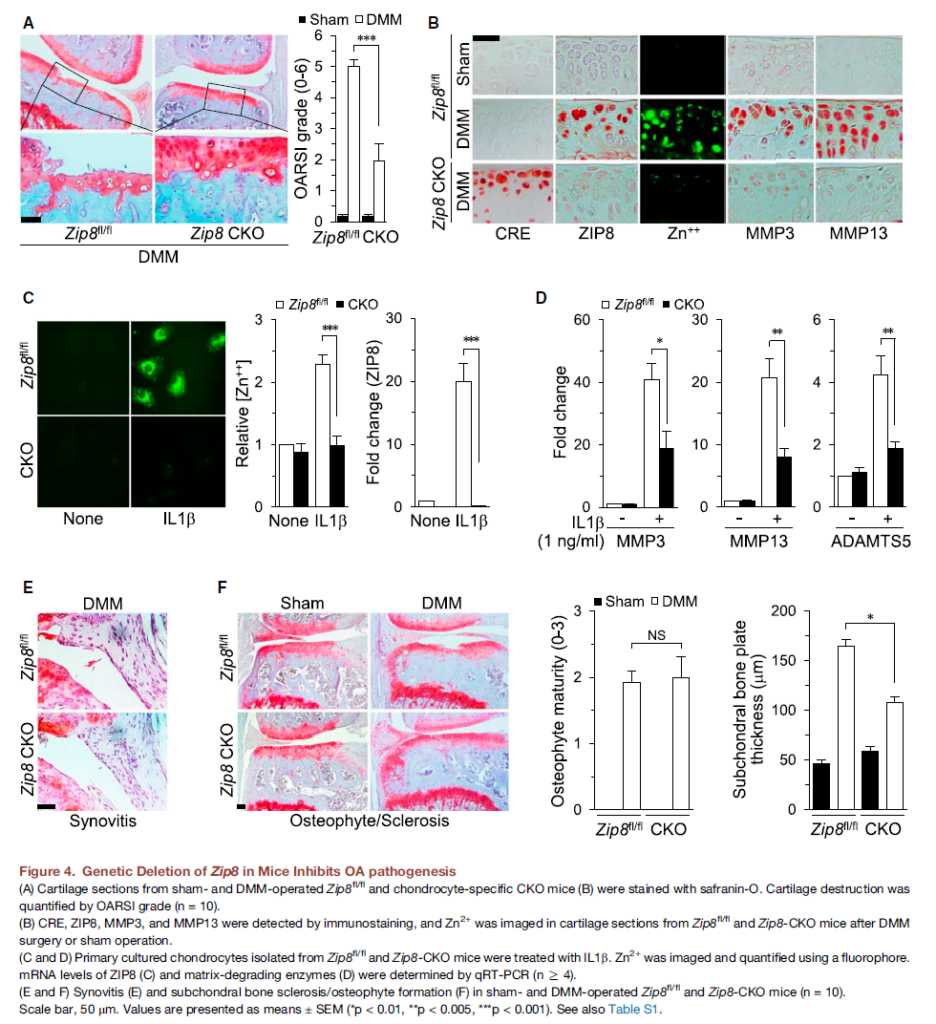
值得注意的是,鋅在 OA 中並非單向有益。研究指出,OA 軟骨中 ZIP8(SLC39A8)鋅轉運蛋白顯著上調,導致細胞內鋅濃度異常升高。此一鋅訊號會活化金屬反應轉錄因子 MTF-1,進而誘導多種基質分解酵素(如 MMP-3、MMP-13)表現,直接加速軟骨基質降解。
此發現揭示鋅在 OA 病理中的關鍵特性:
鋅並非單純的「保護因子」,而是一種需被精密調控的訊號元素。
鋅濃度、細胞內分布、以及轉運蛋白的表現狀態,將共同決定其最終生物效應。
臨床與流行病學層面的鋅與 OA 關聯性
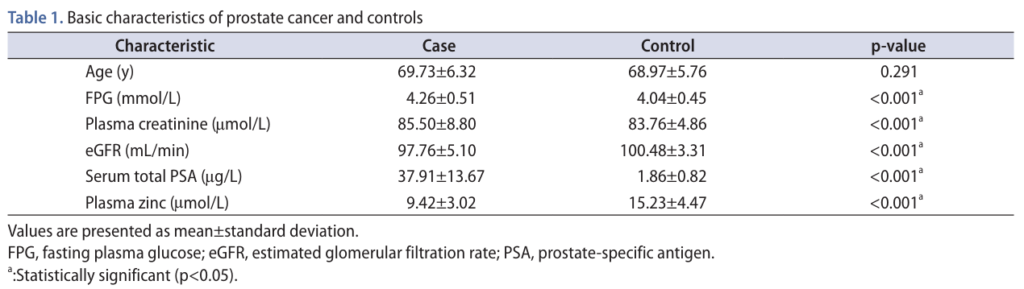
為進一步釐清鋅與退化性關節炎之間的關係是否僅為相關性,Gao 等人於 2025 年採用雙樣本孟德爾隨機化分析,利用遺傳變異作為工具變數,以評估鋅水平對 OA 風險的潛在因果影響。研究結果顯示,不同 MR 分析方法均支持鋅相關遺傳變異與 OA 風險之間存在顯著關聯,顯示鋅水平本身可能位於 OA 發病的因果鏈之中。值得注意的是,該分析反映的是終生暴露於特定鋅水平的遺傳效應,而非短期補充或治療介入,進一步凸顯鋅在 OA 中的角色可能與其長期動態調控密切相關。(Gao et al., Biological Trace Element Research, 2025)
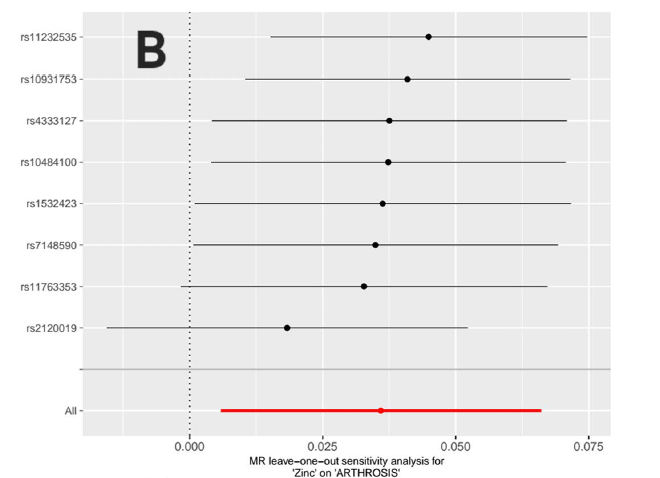
在人群研究中,鋅與 OA 之間的關聯呈現高度複雜性。部分觀察性研究顯示,鋅攝取不足與關節功能惡化相關;研究指出,遺傳決定的鋅代謝變異,與 OA 風險之間存在顯著因果關聯 (整體因果估計呈現正向)。這類研究的價值在於排除混雜因子影響,進一步支持「鋅動態失衡」可能參與 OA 發病機制,而非僅是疾病後果。
鋅於 OA 管理中的應用潛力與挑戰
綜合近年之細胞、動物與臨床研究,鋅在退化性關節炎中的作用並非單向,而呈現高度動態且情境依賴的特性。Tekeoglu 與 Şahin 於 2025 年發表之綜述指出,適當範圍內的鋅有助於維持抗氧化防禦與免疫穩定,藉由支持 Cu/Zn-SOD 活性與 Nrf2 訊號,降低活性氧與慢性發炎對軟骨細胞的傷害。然而,當鋅的細胞內動態失衡,特別是在鋅轉運蛋白異常上調的情況下,過量的游離鋅反而可能透過金屬反應轉錄因子活化,促進基質分解酵素表現,加速軟骨退化。此一雙向效應說明,鋅於 OA 中的潛在治療價值,關鍵不在於單純補充,而在於是否能精準調控其生物可用度與訊號強度。(Figure 1. Tekeoglu & Şahin, 2025.)
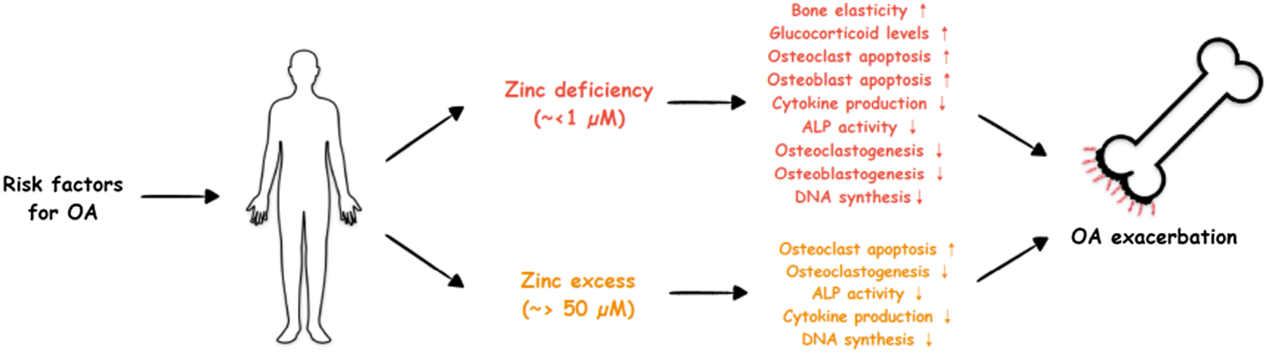
現有證據顯示,鋅在 OA 中同時具有保護性與促退化性潛能,其關鍵不在於是否補充鋅,而在於:
- 鋅的 生物可用度
- 鋅在組織中的 釋放速率
- 是否能避免局部過量鋅訊號的產生
因此,未來 OA 的營養與輔助治療策略,應朝向「精準投予與調控鋅訊號」的方向發展,而非傳統高劑量、非定向的補充模式。
結論
鋅在退化性關節炎中扮演關鍵而多面向的調控角色。適當的鋅訊號有助於抑制氧化壓力與慢性發炎,維持軟骨細胞功能;然而,鋅動態失衡或不當累積,則可能反向促進基質分解與關節退化。整體而言,鋅在 OA 的應用潛力,取決於是否能以精準方式調控其生物可用度與作用時序。此一概念亦為未來 OA 預防與輔助治療策略,提供重要的研究與產業發展方向。
FAQ 常見問題
1.鋅對退化性關節炎到底是好還是壞?
鋅在 OA 中並非單向有益或有害,而是依其濃度、細胞內分布與訊號調控狀態而定。適當的鋅訊號有助於抗氧化與免疫穩定,但鋅動態失衡可能促進基質分解。
2.補充鋅可以改善退化性關節炎嗎?
目前證據顯示,鋅的角色較接近「風險調節因子」,而非直接治療因子。研究強調鋅訊號的精準調控,比單純高劑量補充更為重要。
3.ZIP8 與鋅在 OA 中的關係是什麼?
ZIP8 是軟骨細胞中的鋅轉運蛋白,在 OA 病理條件下上調,可能導致細胞內鋅訊號過度活化,進而啟動基質分解相關基因表現。
4.孟德爾隨機化研究代表什麼意義?
孟德爾隨機化分析利用遺傳變異作為工具,顯示鋅水平與 OA 風險之間存在因果關聯,但不等同於短期補充鋅的治療效果。
參考文獻(國際期刊)
- Tekeoglu, İ., & Şahin, Ş. (2025). The influence of zinc levels on osteoarthritis: A comprehensive review. Nutrition Research Reviews, 38(1), 282–293.
- Amhare, A. F., Liu, H., Qiao, L., Deng, H., & Han, J. (2025). Elemental influence: The emerging role of zinc, copper, and selenium in osteoarthritis. Nutrients, 17(13), 2069.
- Kim, J. H., et al. (2014). Regulation of the catabolic cascade in osteoarthritis by the zinc-ZIP8-MTF1 axis. Cell, 156(4), 730–743.
- Gao, T. Q., et al. (2025). The causal relationship between zinc and osteoarthritis: A two-sample Mendelian randomization study. Biological Trace Element Research.