自然科學雜誌(Nature)旗下的Nanotechnology於2016年發表的研究,將經由FDA安全認證原本一種用於治療「缺鐵性貧血」的藥物,卻意外發現可以有很好的抗腫瘤功效,也造成醫界熱烈討論和轟動。
這藥物中的「鐵」分子進入身體後,會啟動原本被癌細胞壓抑的自身抗癌機制,透過活化免疫系統中具有「腫瘤殺手」之稱的M1巨噬細胞,直接狙殺癌細胞。
巨噬細胞大致分為M1及M2兩型。 M1巨噬細胞主要與發炎、吞噬、攻擊相關。M2巨噬細胞則參與了抗發炎、清理受傷組織、促進血管增生(幫助修復組織);但在遇到腫瘤時,也會因為免疫系統被壓抑,反而促進了腫瘤的生長和轉移。
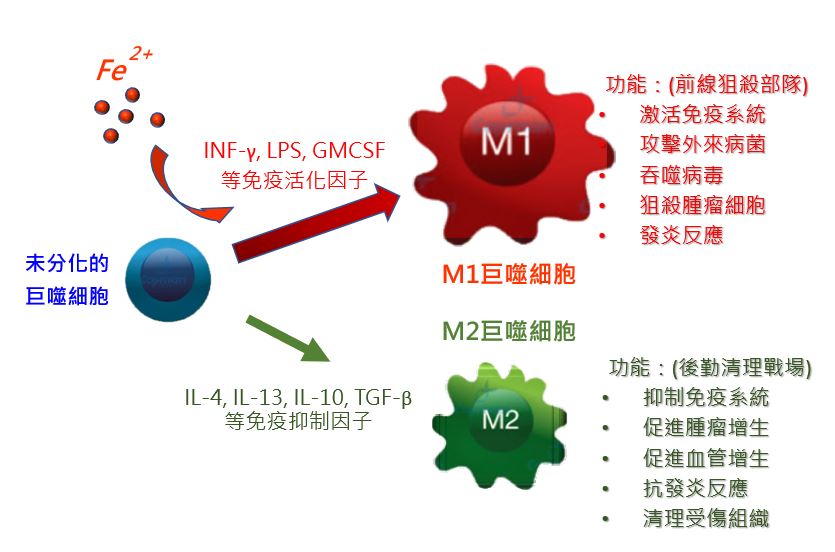
FAAC 誘導M1巨噬細胞的增生與分化
研究人員測試是否能抑制小細胞肺癌的肝轉移。當癌細胞被注射入小鼠體內生長一周後,小鼠開始產生病變,開始用藥可以顯著的阻止癌細胞繼續生長,同時實驗組在肝臟腫瘤周邊,還可以發現大量活化的巨噬細胞;對照組(左)和實驗組(右)比對,第二週就可以看出兩組癌細胞生長不同。
若在注射癌細胞前4天給予藥物,也具有同樣效果,也可在組織間發現活化巨噬細胞的聚集、同時腫瘤的生長就受到控制。
實驗到第三週就更加明顯。
利用生物螢光成像(Bioluminescence imaging)偵測小細胞肺癌細胞的肝轉移程度,如果螢光越強,代表癌細胞越多。由圖可見,接受注射的癌細胞生長受到顯著抑制。
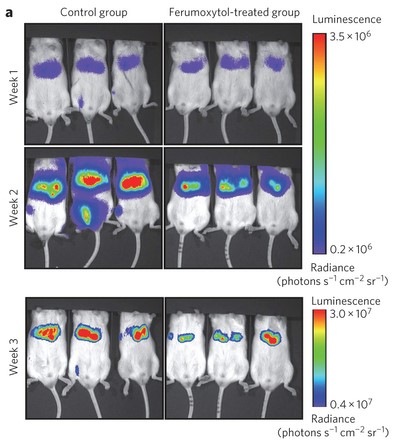
抑制癌細胞擴散小鼠實驗
從研究可觀察到三個現象:
1.本藥物可以刺激誘導大量的M1巨噬細胞生成
2. M1巨噬細胞會辨識並且聚集在腫瘤周圍,直接攻擊癌細胞
3. 腫瘤內同時也會產生大量氧化自由基,誘導癌細胞死亡
參考資料:
1. FDA-approved ferumoxytol displays anti-leukaemia efficacy against cells with low ferroportin levels, Nat Nanotechnol. 2019 Jun; 14(6): 616–622.
2. Tumour-associated macrophages are a distinct M2 polarised population promoting tumour progression: Potential targets of anti-cancer therapy, European Journal of Cancer, Volume 42, Issue 6, April 2006, Pages 717-727.

