作為人體所需的巨量營養元素,補充鎂有益於多種醫療狀況,例如發炎、骨再生、心律不整和憂鬱症。鎂的恆定受到循環系統的調節,攝取過量可藉由糞便和尿液排出體外,因此,鎂累積於人體產生的負面作用非常少見。本文將探討補充鎂,對於預防與治療癌症的應用潛力。
補充鎂減少肺癌風險
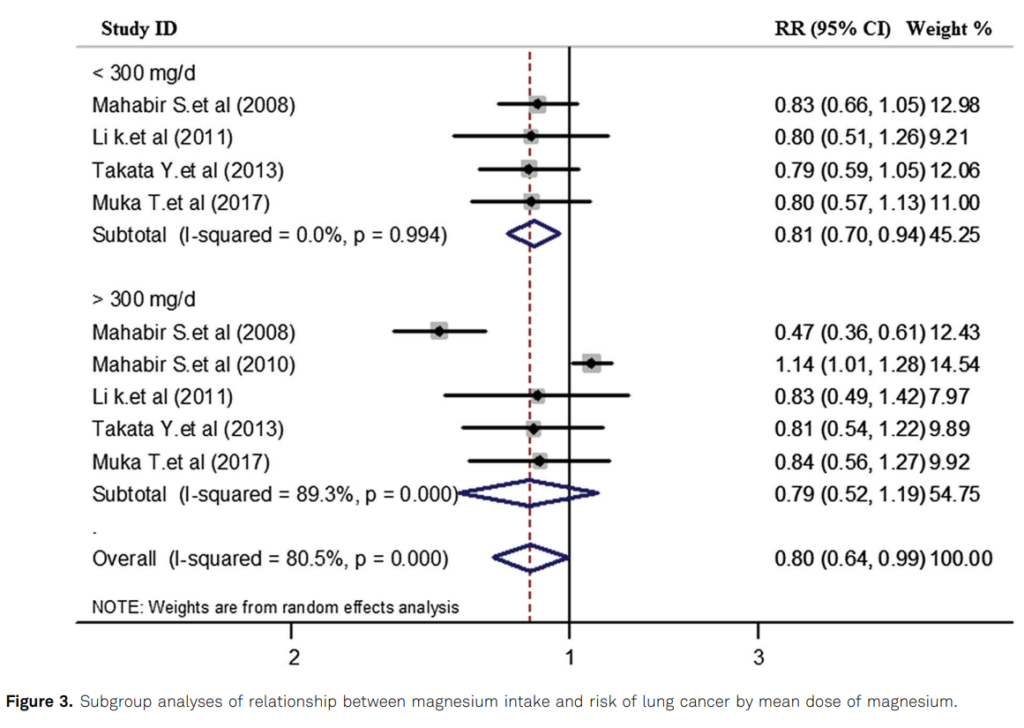
下表來自2021年的期刊1,目的是評估鎂攝取量與肺癌風險之間的關聯,研究共分析了585821 名參與者與8977 例肺癌病例。結果顯示,肺癌發生率與鎂攝取量之間存在相關性,鎂攝取劑量低於 300 mg/day 已能顯著降低肺癌風險(RR = 0.83,p = 0.034),攝取量若增加到 300 mg/day 以上,降低肺癌風險的效果不會更高(RR = 0.89, p = 0.076)。上述分析說明,鎂攝取量低於 300 mg/day 對於肺癌已具有保護作用。
補充鎂抑制直腸癌細胞生長
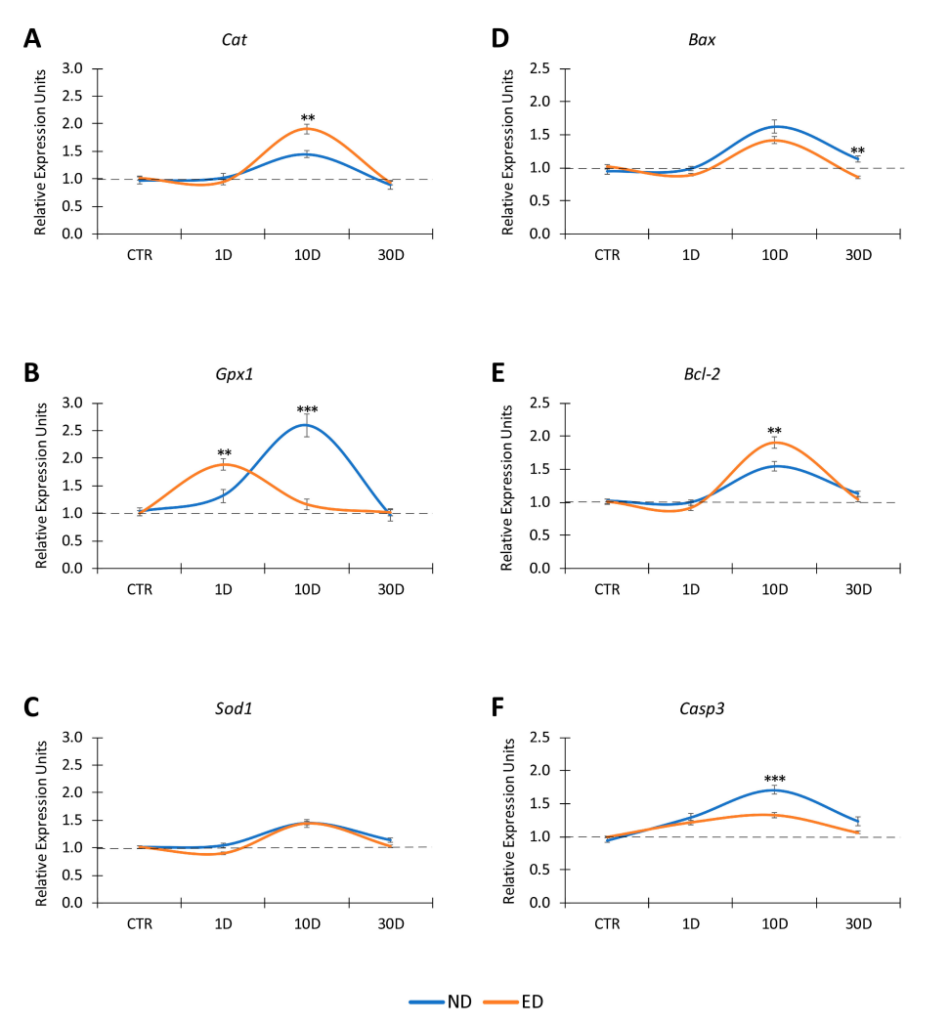
下圖來自2023年的期刊2,目的為探討高濃度的鎂離子對於直腸癌細胞的影響。螢光染色的結果顯示,鎂離子濃度達到 30 mM 時,可以活化 caspase-3,誘導癌細胞凋亡。
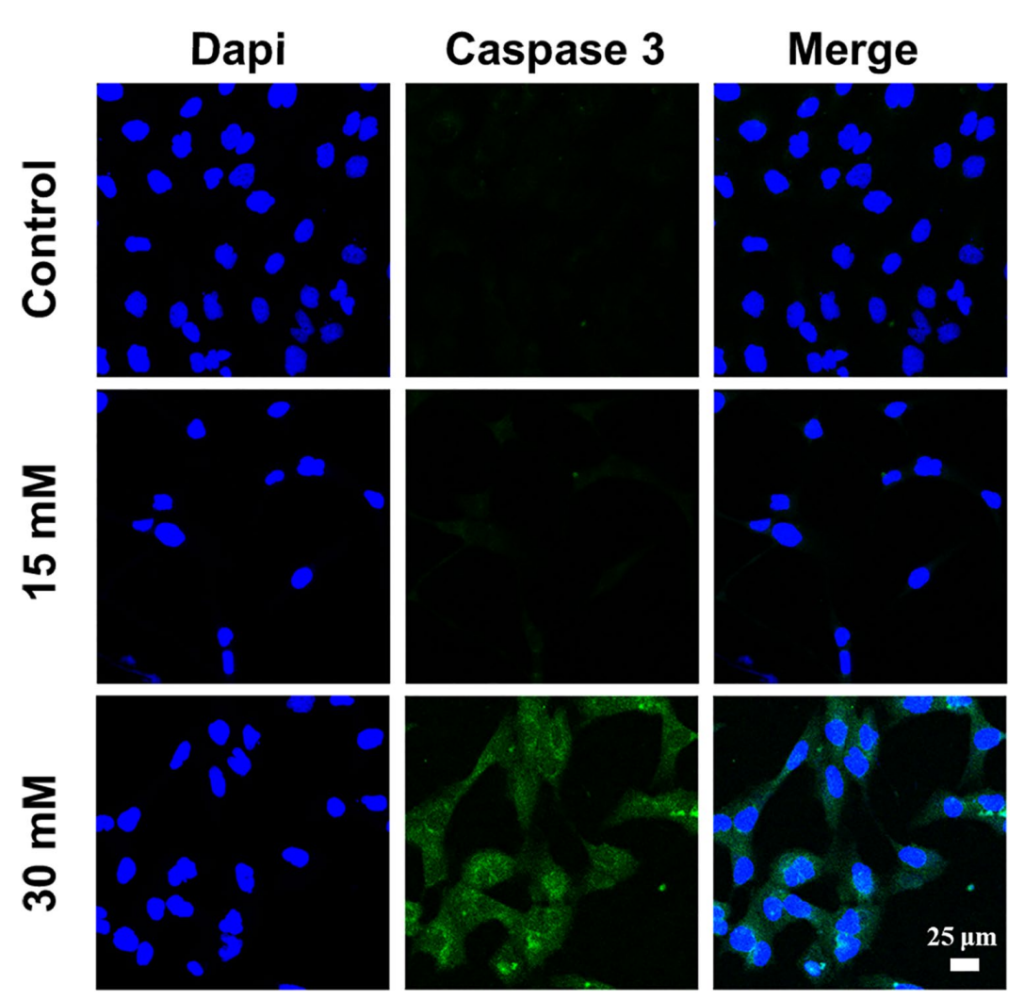
同論文的另一張圖,利用直腸癌荷瘤小鼠動物進行評估,氯化鎂以注射模式投予(500 mM,10 mL),三天一次,共治療3週。與對照組比較,治療組顯著抑制腫瘤生長,其效果可能歸因於鎂離子促進直腸癌細胞的凋亡。
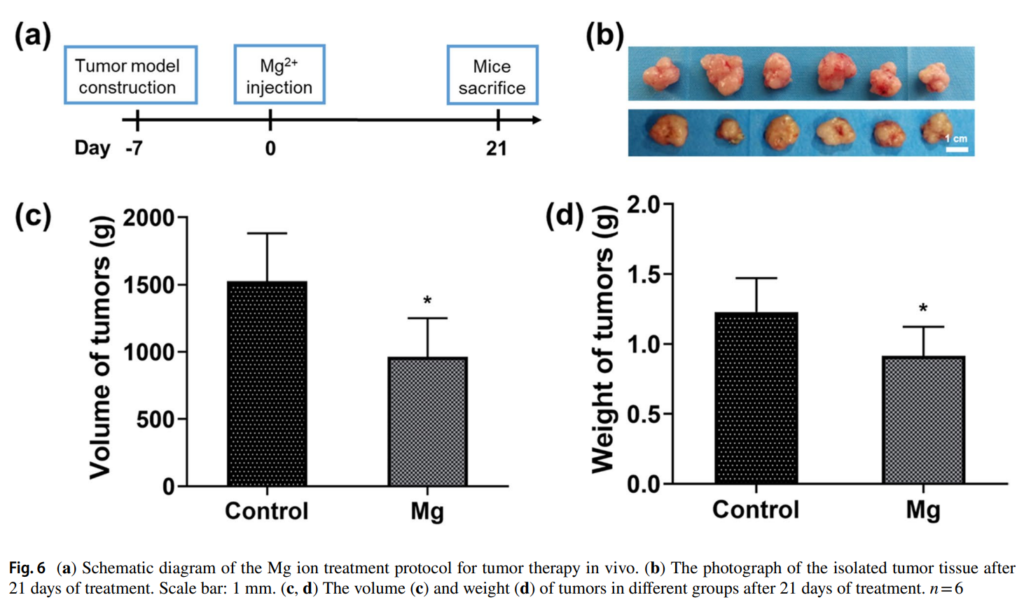
鎂的植入物可抑制膽囊癌
膽囊癌在早期階段很難被發現,而且很容易發生轉移,引起膽管阻塞,此時臨床治療方式為支架植入。然而,常用的膽管支架不可降解,不僅容易發生二次阻塞,還需要二次清除手術。下圖來自2021年的期刊3,目的為探討鎂作為膽管支架的可行性與好處。體外實驗使用高純度的鎂絲,置於7.5、7.8、8.1三種酸鹼值,以模擬弱鹼性的膽汁,並分析其降解產物對於膽囊癌細胞SGC-996的生長影響。在pH 7.8的降解產物,可誘發膽囊癌細胞產生22%的凋亡,具有顯著差異,其效果近似於30 mM的鎂離子;在pH 8.1的降解產物,誘發膽囊癌凋亡的效果更是提升到38%,而pH 8.1恰為膽汁常態酸鹼值範圍的中間值。
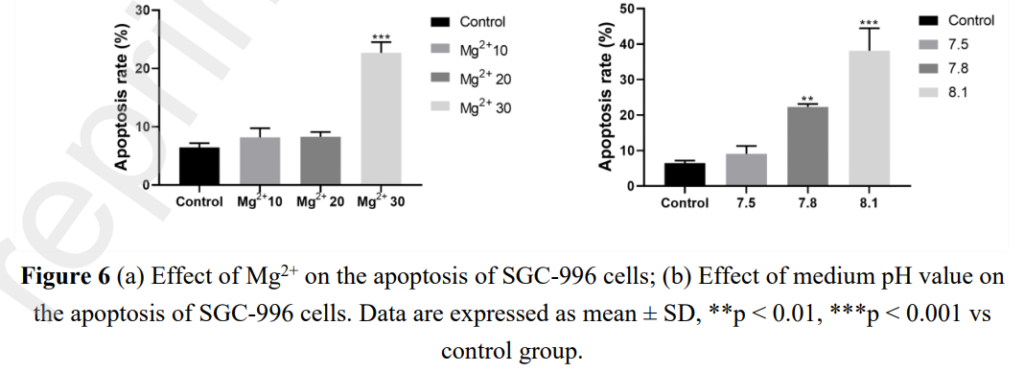
同論文的另一張圖,則利用荷瘤動物實驗探討高純度鎂絲對膽囊癌的影響。使用鈦絲的組別與對照組相較,其抑制膽囊癌的效果無顯著差異;使用鎂絲的組別,與對照組相較則產生顯著差異,且三條鎂絲的效果優於一條鎂絲,具有劑量效應。上述結果揭示鎂支架不論是在生物降解性,或者是抑制膽囊癌效果,均有良好的膽道外科應用前景。
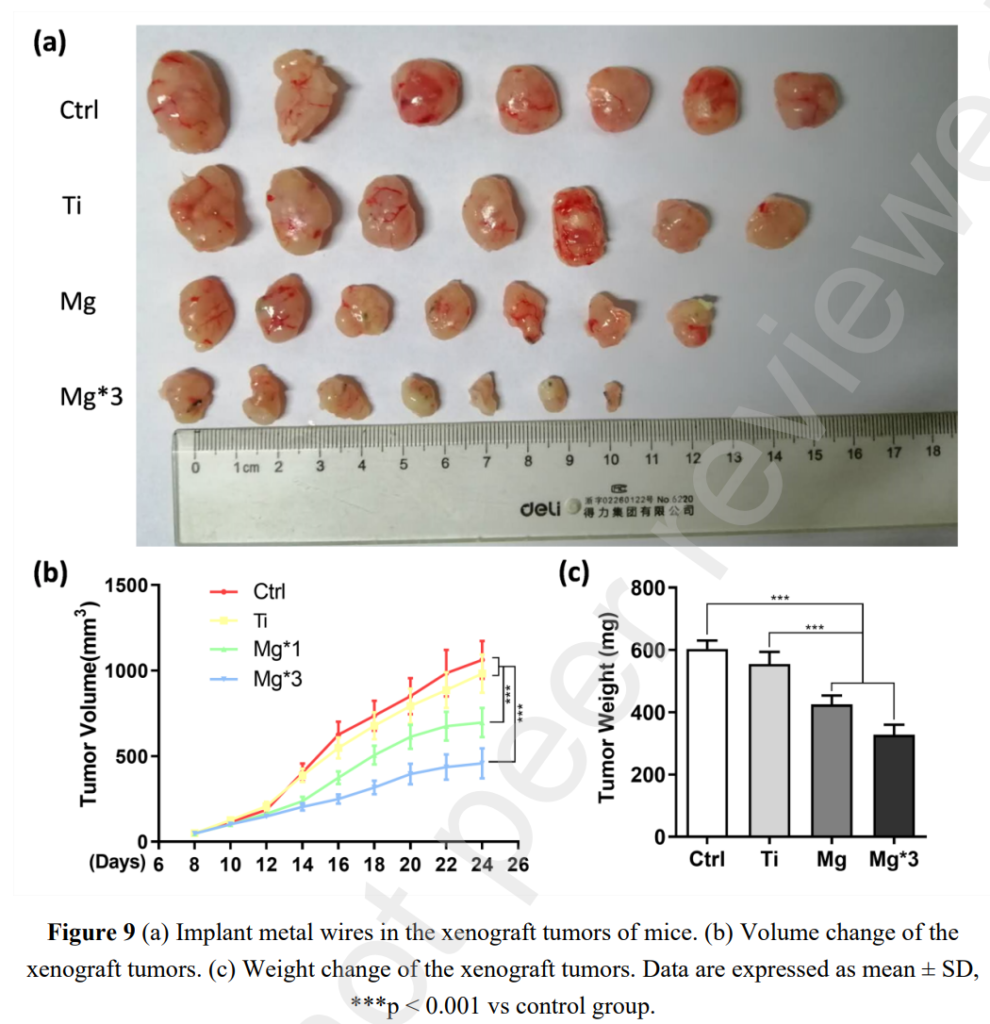
補充鎂提升抗癌免疫力
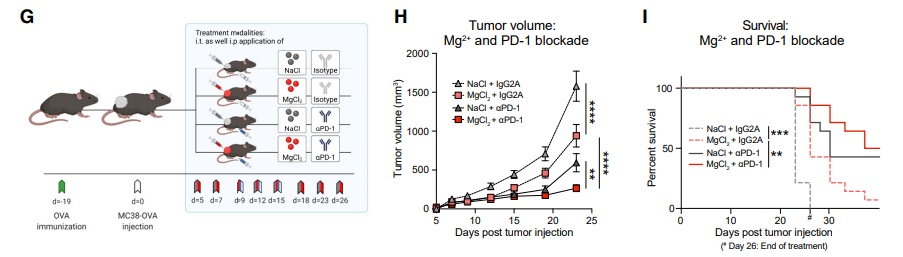
補充高濃度的鎂或植入高純度的鎂應用於治療癌症,機轉大多與誘發癌細胞凋亡相關。至於鎂提升抗癌免疫力的科學證據,則是在近年(2022年)發表於Cell期刊的一篇重磅論文4,開始被學者探討。LFA-1 (leukocyte function-associated antigen 1) 是CD8+ T 細胞的表面分子,與免疫反應的白血球活化、移動相關。當鎂離子與LFA-1結合,可改變LFA-1的構型與親和力,增強T細胞抵抗病原體以及腫瘤的特異性免疫反應。下圖是氯化鎂與anti-PD-1抗體合併使用的動物試驗,概述如下: 1、投予anti-PD-1抗體組別,與投予IgG2A抗體組別相較,抗腫瘤效力提升。2、投予氯化鎂的組別,與投予氯化鈉組別相較,抗腫瘤效力提升。3、氯化鎂合併anti-PD-1抗體的組別,效果比投予anti-PD-1的組別更佳。上述結果說明,鎂離子具有抗腫瘤功效,且能夠提升anti-PD-1的抗癌免疫力,延長存活期。
總結:
對於健康的人而言,補充適量的鎂(<300 mg/day),即有助於降低肺癌風險;對於癌症病人而言,低血清鎂水平意謂癌症發展更快、總生存期更短,因此必須搭配血清鎂的檢測來補充鎂。高濃度的鎂(30 mM),經由細胞試驗與細胞試驗,證實能透過誘導癌細胞凋亡,抑制腫瘤的發育;高純度的鎂,則可以用於生產可降解的新穎醫材,比如說膽管支架,同時能控制膽囊癌的進程。
近幾年的癌症治療顯學是免疫療法,如癌症病人符合基因檢測之標準,免疫療法通常會是醫生推薦給病人的最佳治療選擇。Anti-PD-1是免疫療法的主流藥物,是以許多藥廠研發中的小分子新藥,在臨床試驗均設定為可增強anti-PD-1抗癌免疫力之合併療法。鎂並非特殊的小分子新藥,而是常見的巨量營養元素,亦能透過結合LFA-1來增強anti-PD-1的抗癌免疫力,因此具有相當重要的臨床意義。未來是否有更多醫師在進行各類型癌症治療時,搭配檢測並精準給予鎂補充劑,值得進一步觀察與確認。

參考文獻:
Nasim Dana, Raheleh Karimi, Marjan Mansourian, Shaghayegh Haghjooy Javanmard, Ismail Laher, and Golnaz Vaseghi. Magnesium intake and lung cancer risk: A systematic review and meta-analysis. Int J Vitam Nutr Res (2021), 91 (5–6), 539–546.
Heng Li, Xiaonan Feng, Hai Li, Shuo Ma, Wei Song, Bao Yang, Tao Jiang, Chun Yang. The Supplement of Magnesium Element to Inhibit Colorectal Tumor Cells.
Biological Trace Element Research (2023) 201:2895–2903.
Hongzhou Peng, Kun Fan, Rui Zan, ZiJun Gong, Wentao Sun, Yu Sun, Jie lou, Jiahua Ni, Tao Suo, Xiaonong Zhang. Degradable magnesium implants inhibit gallbladder cancer. Acta Biomaterialia Volume 128, 1 July 2021, Pages 514-522.
Jonas Lo¨ tscher, Adria`-Arnau Martı´ i Lı´ndez, Nicole Kirchhammer, Carolyn G. King, Alfred Zippelius, Christoph Hess. Magnesium sensing via LFA-1 regulates CD8+ T cell effector function. Cell Volume 185, February 17, 2022, Pages 585–602.