自體免疫系統。紅斑性狼瘡、僵直性脊椎炎、類風濕性關節炎、血管炎
痛風是常見的發炎性關節疾病,造成痛風的直接原因是高尿酸。超過12%的痛風患者,是由於遺傳性的基因突變,使得尿酸排泄不足或過量產生。其餘痛風患者多由飲食過於豐盛誘發,愛吃紅肉、內臟、海鮮,搭配飲用啤酒和高果糖飲料,都會增加痛風的風險。痛風的病理特徵,是尿酸鈉晶體在關節間隙沉澱,並觸發免疫反應,釋放發炎細胞因子,導致持續疼痛和關節變形。蹠趾關節最常受痛風影響,其他常見部位包含腳踝、膝蓋、手指、手腕和肘部。
高尿酸與代謝症候群之關聯性
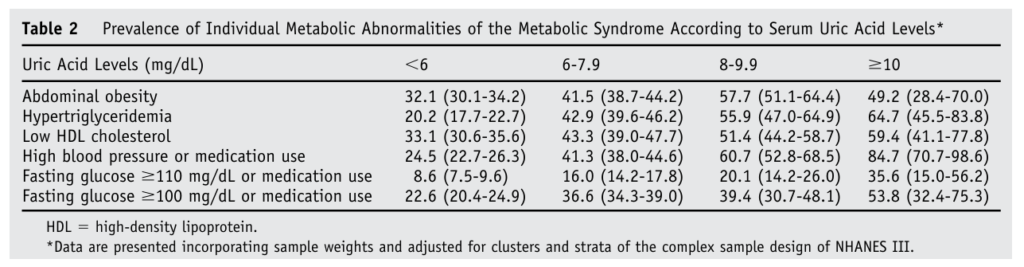
下表來自2007年的期刊1,研究納入8669名20歲以上參與者,分析代謝症候群與尿酸濃度的關聯性。結果顯示,尿酸濃度小於 6 mg/dL 時,代謝症候群發生率為 36.0%;尿酸濃度為 8 ~ 8.9 mg/dL,發生率則提升至62.0%;尿酸濃度大於 10 mg/dL時,代謝症候群發生率高達 70.7%。由上述數據推測,高尿酸血症是代謝症候群的常見合併症,血清尿酸水平可做為評估代謝症候群風險的常規指標。
治療與預防痛風的藥物
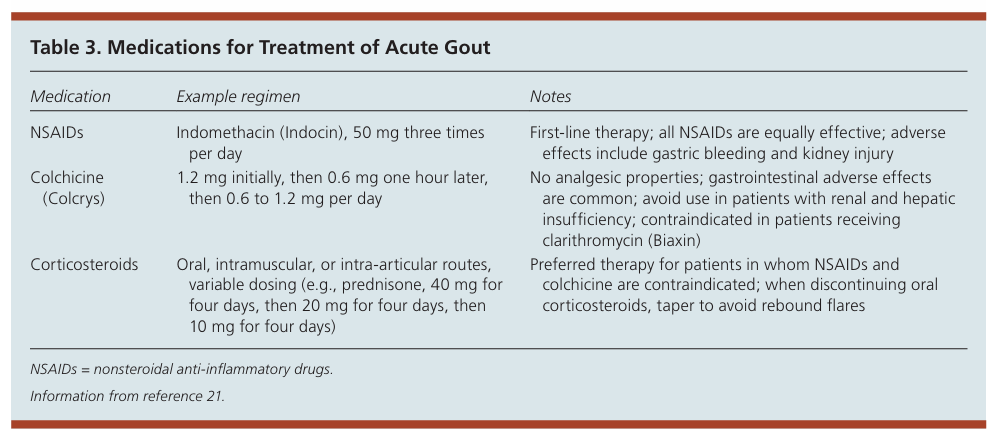
痛風通常使用美國風濕病學會的臨床標準進行診斷,透過鑑定受影響關節滑液中的單鈉尿酸鹽晶體來確診。下表來自2014年的期刊2,描述了急性痛風的用藥,包含: 非類固醇類抗發炎藥、皮質類固醇或秋水仙鹼。為了快速徹底解決症狀,急性痛風的治療應在症狀出現 24 小時內,使用非類固醇抗發炎藥(NSAID)、皮質類固醇和秋水仙鹼。若痛風僅限於單一關節時,關節內注射皮質類固醇是比口服抗發炎藥物更好的策略。在急性期皮質類固醇治療停止後,為了降低反彈風險,須逐漸減少皮質類固醇療程。秋水仙鹼則是急性痛風的另一種治療選擇,但不良反應稍多,包括噁心、嘔吐和腹瀉,因此肝病或腎病患者須慎用。
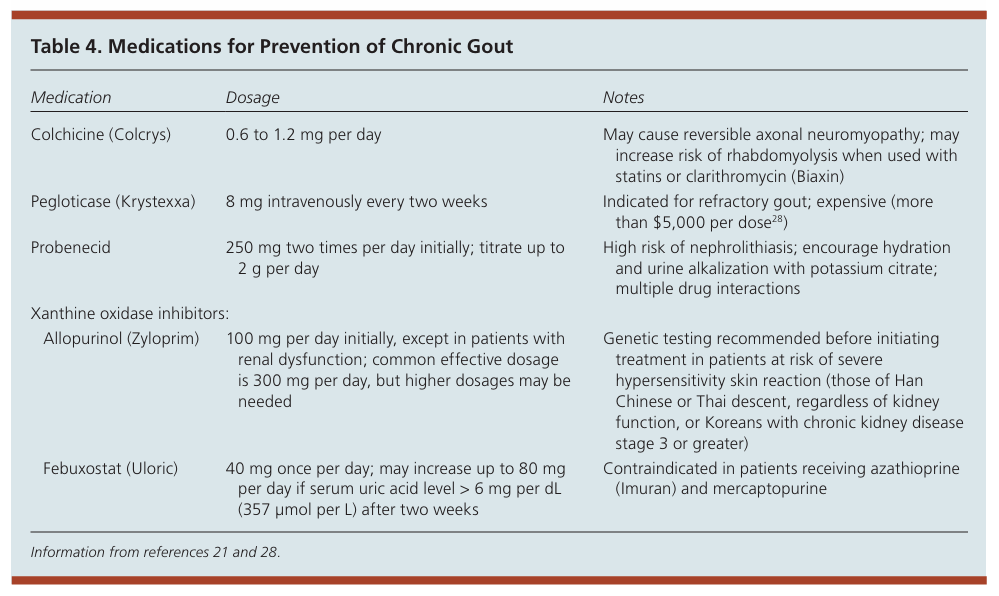
為了減少痛風復發的可能性,患者除了飲食控制外,還有若干藥物建議持續使用。Allopurinol則可抑制尿酸的合成,是預防痛風復發的第一線藥物;Probenecid可增加尿液中尿酸的排泄;Pegloticase可增加尿酸的分解;秋水仙鹼和Febuxostat則保留給不能耐受一線藥物或第一線藥物無效的患者。對於沒有痛風石的患者,在尿酸水平低於目標後,治療應持續至少三個月;對於有痛風石的患者,治療應持續六個月。
膳食鎂有助於預防高尿酸
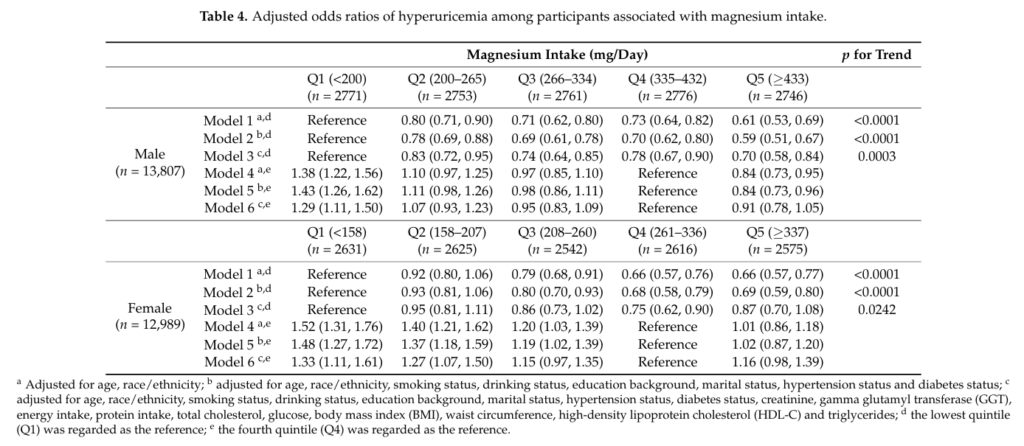
下表來自2018年的期刊3,研究納入26796名美國成年人,透過多變量迴歸模型,評估膳食鎂攝取量與高尿酸血症之間的關聯。男性的數據顯示,第一個五分位數(Q1)的尿酸血症相對機率(OR)最高,是第四個五分位數(Q4)的1.29 倍;女性第一個五分位數(Q1)的OR同樣最高,為第四個五分位數(Q4)的1.33倍。上述結果表明,增加鎂攝取量可降低高尿酸血症風險,有助於預防高尿酸血症。
補充鎂降低高尿酸與痛風患者之死亡率
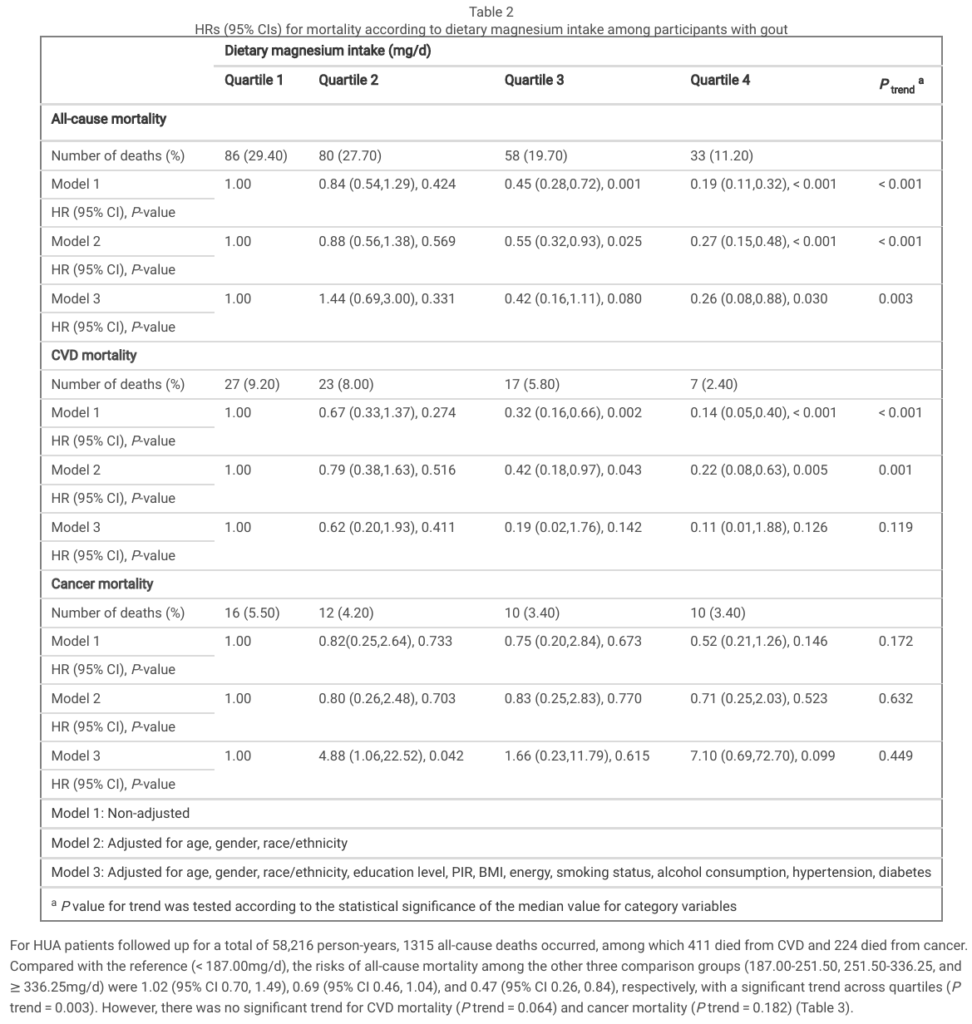
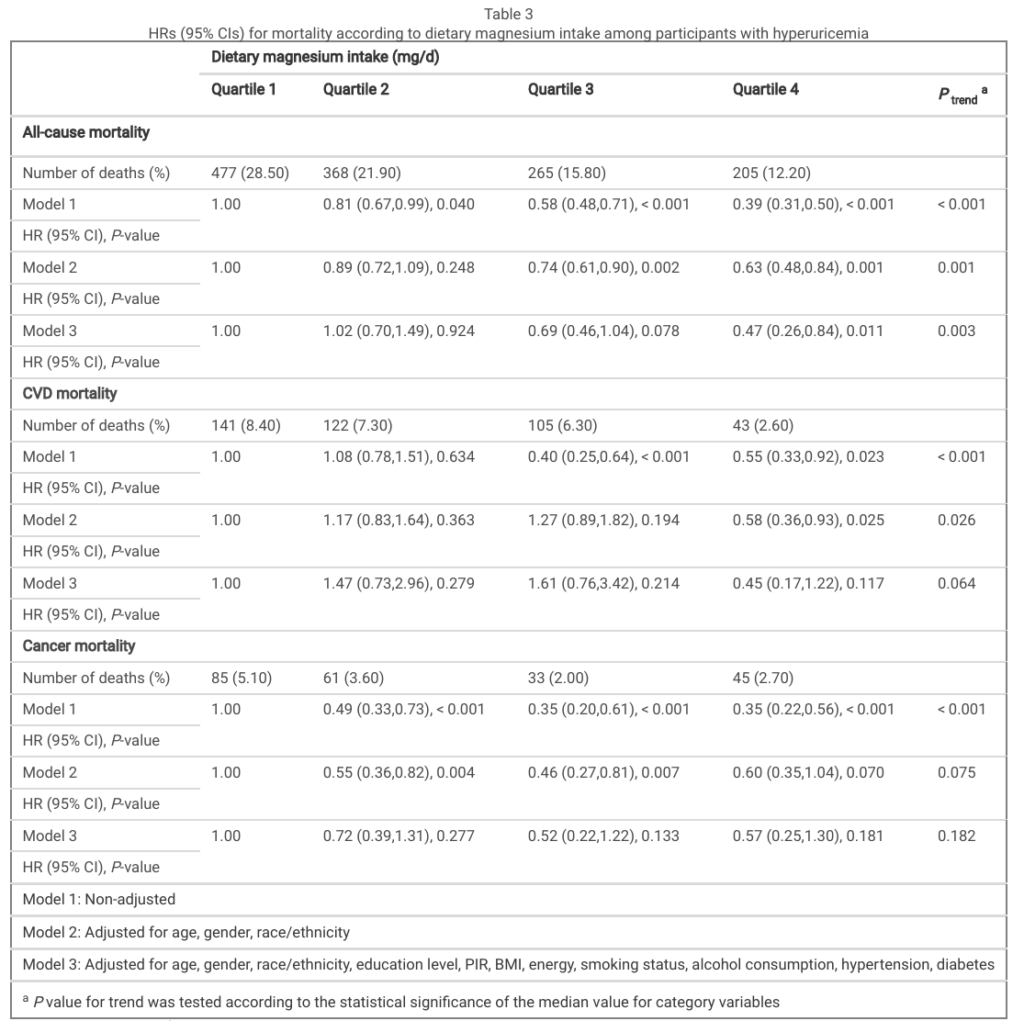
下表來自2024年的期刊4,研究納入1171名痛風患者和6707名高尿酸血症患者,使用Cox迴歸模型,評估飲食鎂攝取量與痛風和高尿酸血症患者死亡率的關係。表二記載共有257名痛風患者死亡,其中74人死於心血管疾病(CVD),48人死於癌症;表三記載共有1315名高尿酸血症患者死亡,其中 411人死於心血管疾病,224人死於癌症。結果顯示,在第四個四分位數的組別(攝取較高的鎂),痛風和高尿酸患者的整體死亡率均降低,心血管疾病的死亡率亦降低。
總結:
流行病學研究顯示,痛風是最常發生的發炎性關節炎之一,其全球盛行率持續在增加。痛風來自於高尿酸血症的邏輯相當明確,因此治療或預防痛風的主要策略,均圍繞著控制尿酸來制定,包含抑制尿酸合成,或增加尿酸排除、分解。文獻亦指出,尿酸的數值與代謝症候群的發生率相關,甚至可將尿酸視為分析代謝疾病風險的指標。由臨床數據進行多變因迴歸分析,發現攝取足夠的膳食鎂,有助於預防高尿酸,並減少高尿酸與痛風患者的死亡率,證明鎂對於高尿酸與痛風患者,能展現正面的效益。未來仍需要更多的機轉探討,來確認鎂改善高尿酸與痛風,是直接發生的事件,或者是由改善代謝疾病而間接促成。
參考文獻:
- Hyon K. Choi, Earl S. Ford. Prevalence of the Metabolic Syndrome in Individuals with Hyperuricemia. The American Journal of Medicine (2007) 120, 442-447.
- BARRY L. HAINER, ERIC MATHESON, and R. TRAVIS WILKES. Diagnosis, Treatment, and Prevention of Gout. American Family Physician Volume 90, Number 12. December 15, 2014.
- Yiying Zhang and Hongbin Qiu. Dietary Magnesium Intake and Hyperuricemia among US Adults. Nutrients 2018, 10, 296.
- Xuanni Lu, Anqi Wang, Ke Liu, Ying Chen, Chen, Yingying Mao, Ding Ye. Associations of dietary magnesium intake with all-cause and cause-specific mortality among individuals with gout and hyperuricemia. Research Square. June 11th, 2024.